Si toma este medicamento, llame a su médico ahora, FDA advierte
Las tabletas contienen niveles de "impurezas por encima de los límites diarios aceptables", según la FDA.
Si estas tomando unibuprofeno de venta libre Para dolores y dolores o una tableta.prescrito por su médico Para una condición a largo plazo, usted banca en el medicamento que consume para que se sienta mejor. Desafortunadamente, en algunos casos raros, las píldoras que está tomando pueden tener el efecto opuesto, que es el caso de un medicamento que la Administración de Drogas (FDA) de EE. UU.anunció un retiro de. Siga leyendo para averiguar si podría verse afectado por el último retiro de receta.
RELACIONADO:Esto es cuando debe tomar Tylenol en lugar de Advil, los médicos dicen.
Se ha retirado un medicamento común de la diabetes.

Más de 1 de cada 10 personas en los Estados Unidos.tener diabetesDe acuerdo con los últimos datos de los Centros para el Control y la Prevención de Enfermedades (CDC). Mientras que hay muchosCambios de estilo de vida recomendados Para aquellos con la condición común, muchas personas con diabetes tipo 2 toman un tipo de medicamento llamado Biguanides para controlar el alto nivel de azúcar en la sangre. Según la línea de salud, laEl tipo más común de biguanida es metformina.. Y ahora, una compañía ha recordado su medicamento de Metformin, la FDA anunció el 11 de junio.
Viona Pharmaceuticals Inc. Se está recuperando voluntariamente dos lotes de tabletas de liberación de hidrocloruro de metformina de hidrocloruro de 750 mg. Los lotes de metformina en cuestión, que se distribuyeron en todo el país, contienen NDC número 72578-036-01, incluyen el número de lote M915601, y tiene la fecha de vencimiento del 2021 de octubre. Los tabletas en sí son blancos para blanco, sin recordar y tienen el Las letras "Z" y "C" en un lado y el número "20" en el otro.
El medicamento contiene altos niveles de carcinógeno.

La metformina se recordó debido a los "niveles de impurezas de nitrosodimetilamina (NDMA) por encima de los límites diarios aceptables".
En el aviso publicado por la FDA, Viona Pharmaceuticals explica que "NDMA se clasifica como un posible carcinógeno humano (una sustancia que podría causar cáncer) según los resultados de las pruebas de laboratorio".
Según la Agencia de Protección Ambiental de los Estados Unidos, "Ndma es un químico orgánico semivolátil Que se forman tanto en procesos industriales como en los naturales ". Está clasificado como un carcinógeno B2, lo que significa que es probablemente que cause cáncer a los humanos, como señala Viona Pharmaceuticals.
RELACIONADO:Si su médico le dio una muestra de este medicamento, no lo use, FDA advierte
Los pacientes que toman la medicación afectada deben comunicarse con su médico.

Viona Pharmaceuticals Inc. no había recibido ningún informe de eventos adversos de salud en el momento en que se emitió el recuerdo de metformina el 11 de junio.
El anuncio de recuperación dice que los pacientes que han recibido las tabletas de metformina afectadas "se recomienda continuar tomando su medicamento y comuníquese con su médico para obtener asesoramiento sobre un tratamiento alternativo". Eso se debe a que, según la FDA, "podría ser peligroso para los pacientes con esta condición grave paraDeja de tomar su metformina. Sin primero hablar con sus profesionales de la salud ".
Viona Pharmaceuticals está notificando a sus clientes por correo electrónico y correo electrónico y está organizando la devolución de todas las tabletas recordadas. Los consumidores con preguntas sobre el retiro pueden llamar a los Servicios de Ciencias de la Vida del Procesador de Recuperación Eversana al 888-304-5022, de lunes a viernes de 8 a.m. a 7 p.m. CONNECTICUT. Aquellos con preguntas relacionadas con la médica deben comunicarse con Viona Pharmaceuticals al 888-304-5011, de lunes a viernes, 8:30 a.m. 5:30 p.m. Et.
Tú también puedesPóngase en contacto con la FDA en línea o por teléfono al 800-332-1088 para reportar una respuesta adversa a la metformina en cuestión.
Esta no es la primera vez que las tabletas de Metformin han tenido este problema.
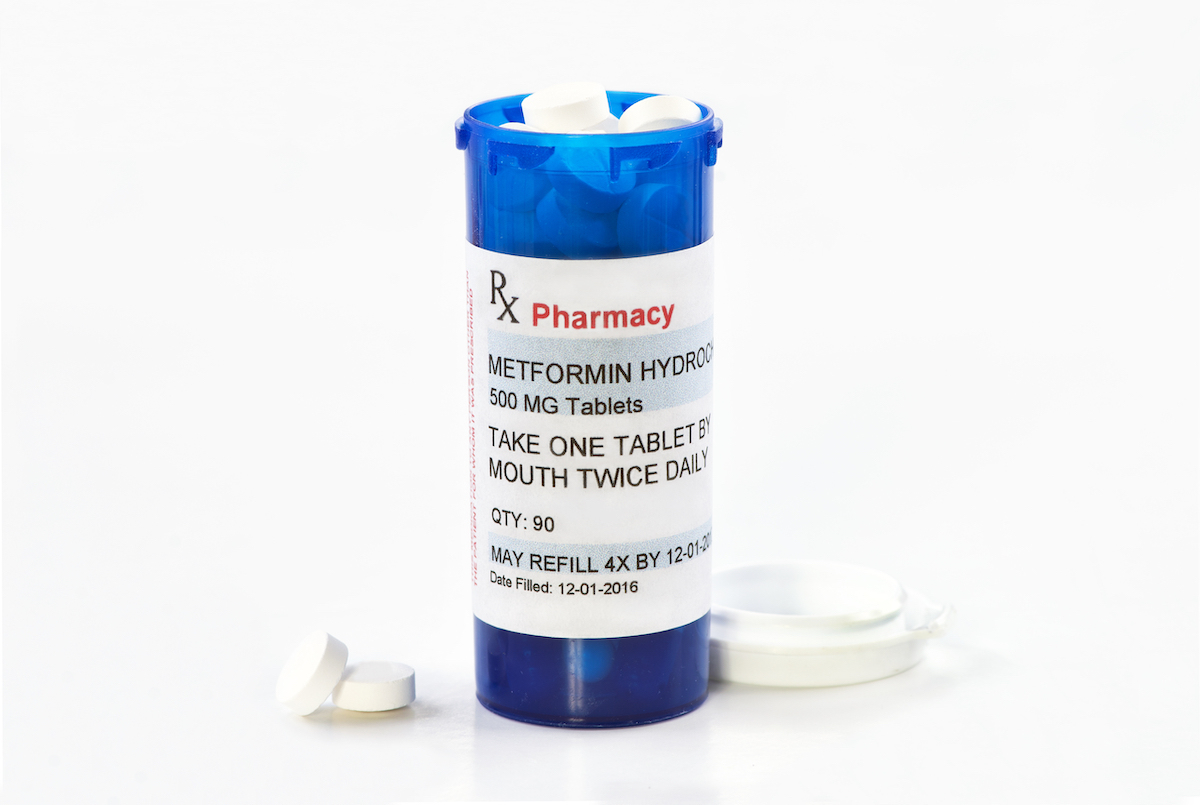
En mayo de 2020, la FDA recomendó que algunas compañías farmacéuticas que realicen tabletas de liberación extendida de metformina.recordarlos debido a los "niveles de NDMA inaceptables".
Muchas empresas, incluyendoPharmacéuticos amnalDeTeva PharmaceuticalsDeApotex corpDeGránulos farmacéuticosDeFarmacéuticos lupinosDeFarmacéuticos BayshoreDeMarksans Pharma LimitedDeSun Pharmaceutical Industries, yLaboratorios de Nostrum-Ha pulsó las píldoras de liberación extendida de Metformin desde el mercado desde esa recomendación de la FDA, todas debido a altos niveles de NDMA.
"La FDA tiene estándares estrictos para la seguridad, la efectividad y la calidad, y la Agencia hace que todos los esfuerzos se basen en la ciencia y los datos para ayudar a mantener a la medida de los Estados Unidos,"Patrizia Cavazzoni, MD, el director interino del Centro de Evaluación de Drogas e Investigación de la FDA en ese momento, dijo en un comunicado. "Ahora que hemos identificado algunos productos de metformina que no cumplen con nuestros estándares, estamos tomando medidas. Como lo hemos estado haciendo, ya que esta impureza se identificó por primera vez, nos comunicaremos a medida que esté disponible una nueva información científica y tomará una acción adicional, si apropiado."
RELACIONADO: Este medicamento podría causar anticuerpos más bajos después de su vacuna COVID, el estudio dice .

Este fotógrafo nos transporta a un planeta de hadas.

