Kung kukuha ka ng gamot na ito, tawagan ang iyong doktor ngayon, nagbabala ang FDA
Ang mga tablet ay naglalaman ng mga antas ng "impurities sa itaas katanggap-tanggap na mga limitasyon sa araw-araw," ayon sa FDA.
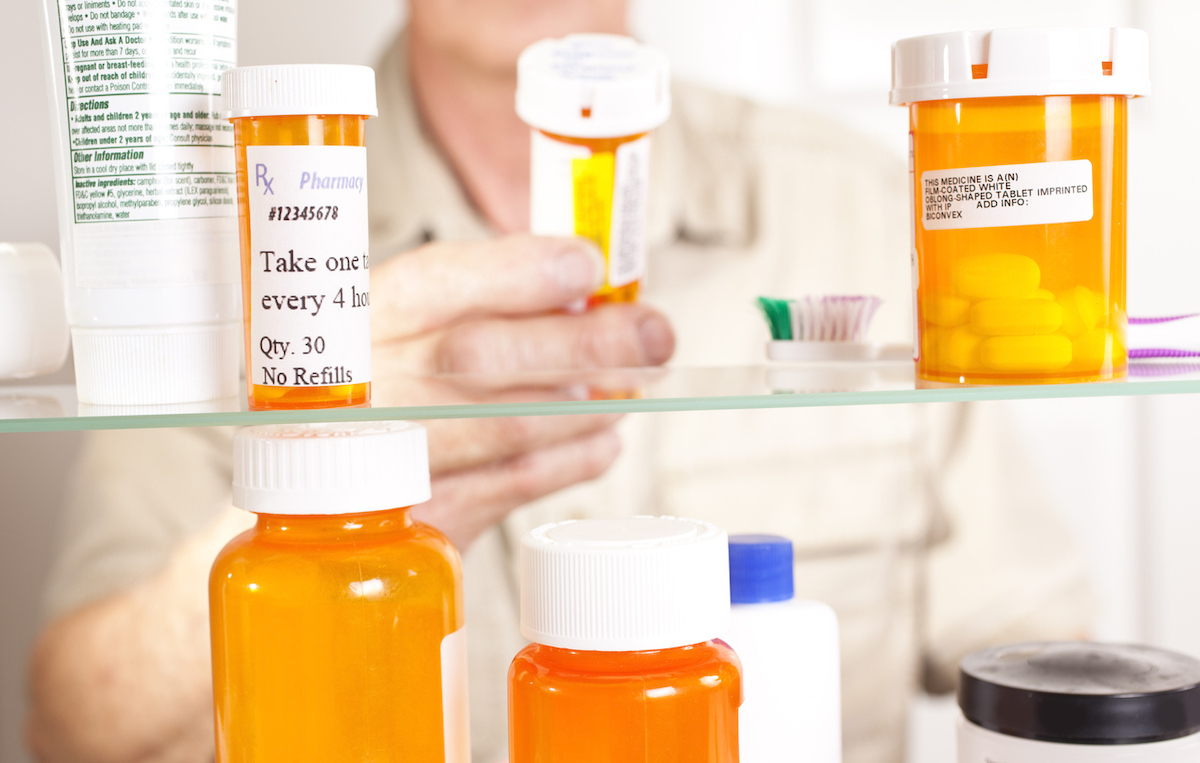
Kung kumukuha ka ng isangOver-the-counter ibuprofen. para sa mga sakit at sakit o isang tabletinireseta ng iyong doktor Para sa isang pang-matagalang kondisyon, ikaw bank sa gamot na ubusin mo upang maging mas mahusay ang pakiramdam mo. Sa kasamaang palad, sa ilang mga bihirang pagkakataon, ang mga tabletas na kinukuha mo ay maaaring magkaroon ng kabaligtaran na epekto, na kung saan ay ang kaso sa isang gamot na ang U.S. Food & Drug Administration (FDA) lamanginihayag ang isang pagpapabalik ng. Basahin ang upang malaman kung maaari kang maapektuhan ng pinakabagong pagpapabalik ng reseta.
Kaugnay:Ito ay kapag dapat mong gawin Tylenol sa halip ng advil, sinabi ng mga doktor.
Ang isang karaniwang gamot sa diyabetis ay naalaala.

Higit sa 1 sa 10 tao sa U.S.may diyabetis, ayon sa pinakabagong data mula sa mga sentro para sa kontrol at pag-iwas sa sakit (CDC). Habang maramingInirerekomenda ang mga pagbabago sa pamumuhay Para sa mga may karaniwang kondisyon, maraming mga taong may uri ng diyabetis ang kumuha ng isang uri ng gamot na tinatawag na Biguanides upang makontrol ang mataas na asukal sa dugo. Ayon sa Healthline, The.Ang pinaka-karaniwang uri ng Biguanide ay metformin.. At ngayon, ang isang kumpanya ay naalaala ang medikasyon ng metformin, inihayag ng FDA noong Hunyo 11.
Viona Pharmaceuticals Inc. ay kusang-loob na recalling dalawang maraming metformin hydrochloride pinalawig-release 750 mg tablet. Ang mga batch ng metformin na pinag-uusapan, na ipinamamahagi sa buong bansa, naglalaman ng Numero ng NDC 72578-036-01, kasama ang Batch Number M915601, at may petsa ng pag-expire na Oktubre 2021. Ang mga tablet mismo ay puti sa off-white, uncoated, at may Mga titik na "Z" at "C" sa isang gilid at ang bilang na "20" sa kabilang banda.
Ang gamot ay naglalaman ng mataas na antas ng isang carcinogen.

Ang metformin ay naalaala dahil sa "mga antas ng nitrosodimethylamine (nDMA) na mga impurities sa itaas ng mga katanggap-tanggap na pang-araw-araw na limitasyon."
Sa paunawa na nai-post ng FDA, ang Viona Pharmaceuticals ay nagpapaliwanag na "ang NDMA ay inuri bilang isang posibleng carcinogen ng tao (isang sangkap na maaaring maging sanhi ng kanser) batay sa mga resulta mula sa mga pagsubok sa laboratoryo."
Ayon sa U.S. Environmental Protection Agency, "NDMA ay isang semivolatile organic na kemikal na bumubuo sa parehong pang-industriya at likas na proseso. "Ito ay inuri bilang isang b2 carcinogen, ibig sabihin ito ay malamang na sanhi ng kanser sa mga tao, tulad ng mga tala ng viona pharmaceutical.
Ang mga pasyente na kumukuha ng apektadong gamot ay dapat makipag-ugnayan sa kanilang doktor.

Ang Viona Pharmaceuticals Inc. ay hindi nakatanggap ng anumang mga ulat ng mga salungat na pangyayari sa kalusugan sa oras na ibinigay ang Metformin Recall noong Hunyo 11.
Ang anunsyo ng pagpapabalik ay nagsasabi na ang mga pasyente na nakatanggap ng mga apektadong metformin tablet "ay pinapayuhan na magpatuloy sa pagkuha ng kanilang gamot at makipag-ugnay sa kanilang manggagamot para sa payo tungkol sa isang alternatibong paggamot." Iyon ay dahil, ayon sa FDA, "maaaring mapanganib para sa mga pasyente na may malubhang kondisyon na itoItigil ang pagkuha ng kanilang metformin. nang hindi kaagad nakikipag-usap sa kanilang mga propesyonal sa pangangalagang pangkalusugan. "
Ang Viona Pharmaceuticals ay nagpapaalam sa mga customer nito sa pamamagitan ng email at mail at nag-aayos para sa pagbabalik ng lahat ng naalaala na mga tablet. Ang mga mamimili na may mga tanong tungkol sa pagpapabalik ay maaaring tumawag sa recall processor Eversana Life Science Services sa 888-304-5022, Lunes hanggang Biyernes mula 8 A.M. hanggang 7 p.m. Ct. Ang mga may mga tanong na may kaugnayan sa medisina ay dapat makipag-ugnayan sa Viona Pharmaceuticals sa 888-304-5011, Lunes hanggang Biyernes, 8:30 A.M. 5:30 p.m. ET.
Maaari mo ringMakipag-ugnay sa FDA online o sa pamamagitan ng telepono sa 800-332-1088 upang mag-ulat ng isang masamang tugon sa metformin na pinag-uusapan.
Hindi ito ang unang pagkakataon na ang mga tablet ng Metformin ay nagkaroon ng isyung ito.
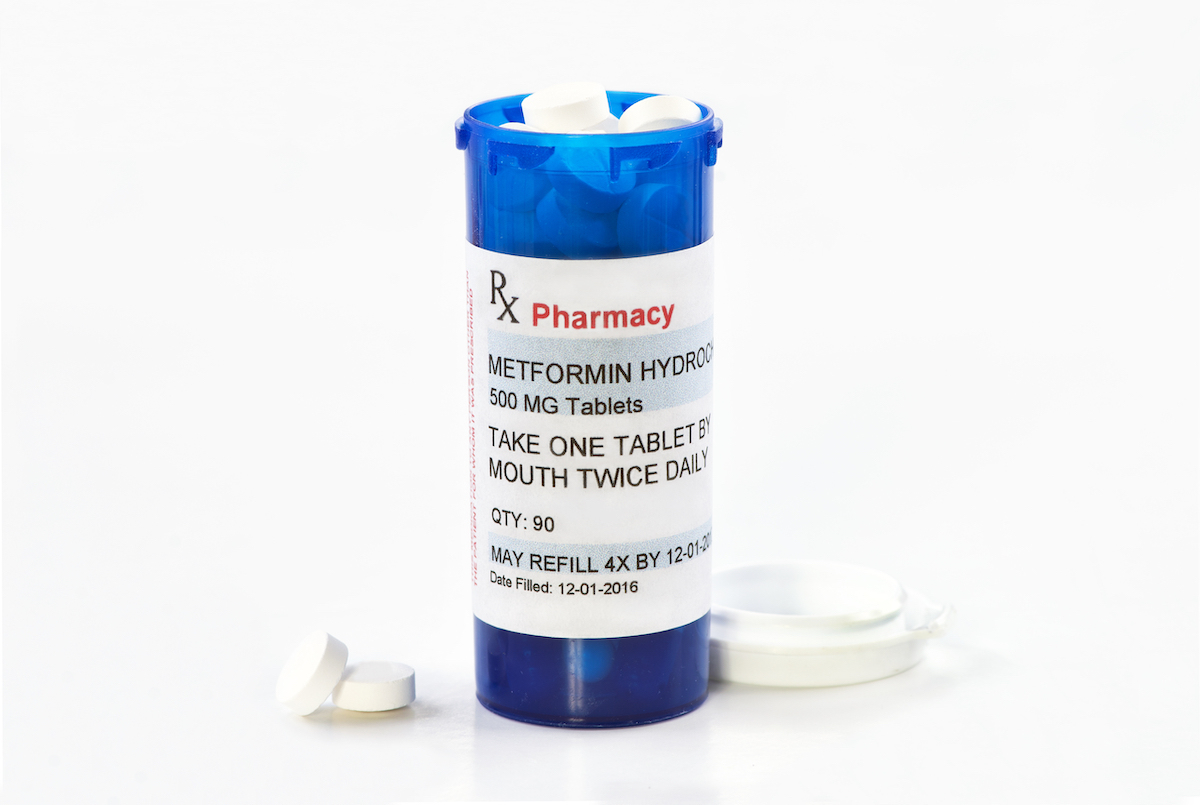
Noong Mayo 2020, inirerekomenda ng FDA na ang ilang mga pharmaceutical company na gumawa ng metformin extended release tabletsAlalahanin ang mga ito dahil sa "hindi katanggap-tanggap na mga antas ng NDMA."
Maraming mga kumpanya-kabilang ang.Amneal pharmaceuticals.,Teva Pharmaceuticals.,Apotex Corp.,Granules Pharmaceuticals.,Lupine pharmaceuticals.,Bayshore Pharmaceuticals.,Marksans Pharma Limited.,Sun pharmaceutical industries., atNostrum laboratories.-Have ang kanilang metformin extended release tabletas mula sa merkado dahil ang FDA rekomendasyon, lahat dahil sa mataas na antas ng NDMA.
"Ang FDA ay may mahigpit na pamantayan para sa kaligtasan, pagiging epektibo at kalidad, at ang ahensiya ay gumagawa ng bawat pagsisikap batay sa agham at data upang makatulong na mapanatiling ligtas ang suplay ng U.S."Patrizia Cavazzoni., MD, ang kumikilos na direktor ng sentro ng FDA para sa pagsusuri at pananaliksik sa droga noong panahong iyon, ay nagsabi sa isang pahayag. "Ngayon na nakilala namin ang ilang mga produkto ng metformin na hindi nakakatugon sa aming mga pamantayan, nagsasagawa kami ng pagkilos. Tulad ng ginagawa namin dahil ang karumihan ay kinilala muna, makikipag-usap kami bilang bagong pang-agham na impormasyon na magagamit at magkakaroon ng karagdagang pagkilos, kung angkop. "

Mabilis na diyeta: Mawalan ng timbang nang mabilis, siyempre at walang stress

