Die neue FDA-genehmigte COVID-Behandlung funktioniert nur für diese Menschen
Diese hilfreiche Behandlung kann tatsächlich für einige Coronavirus-Fälle schädlich sein.

Ein weiterer Schritt in den Kampf gegen Coronavirus wurde von der US-amerikanischen Food and Drug Administration (FDA) zur Notfallgenehmigung genehmigt. Am 9. Februar verabreicht Eli Lillys Antikörper-Bamlanivimab und Etesevimab zusammenerhalten Genehmigung. Die Behandlung kann schwenkbar sein, wenn Menschen mit COVID schneller erholt werden. Es ist jedoch nicht für jeden. Lesen Sie weiter, um die Anwendungen und Einschränkungen dieser Coronavirus-Behandlung zu lernen, und um sicherzustellen, dass Sie gesund bleiben,Wenn Sie über 65 sind, könnten Sie dieses Covid-Symptom vermissen, das Studium sagt.
Die neue FDA-genehmigte COVID-Behandlung wird nur für bestimmte Personen empfohlen.
Um diese neu genehmigte Behandlung zu erhalten, müssen Sie in eine der von Eli Lilly umrissenen Gruppen und der FDA fallen. Menschen, die positiv für Covid testen und habenleichte bis mittelschwere Symptome Oder sind es ein hohes Risiko für die Fortschritte bei schwerer COVID oder der Krankenhausaufenthalt, ist für diese Behandlung geeignet. Darüber hinaus können die Leuten der FDA die Behandlung nur die Behandlung erhalten, wenn sie 12 Jahre oder älter sind, und wiegen mindestens 88 Pfund. Und für mehr aktuelle Informationen,Melden Sie sich für unseren täglichen Newsletter an.
Menschen, die bereits im Krankenhaus sind, sind nicht für die Behandlung geeignet.
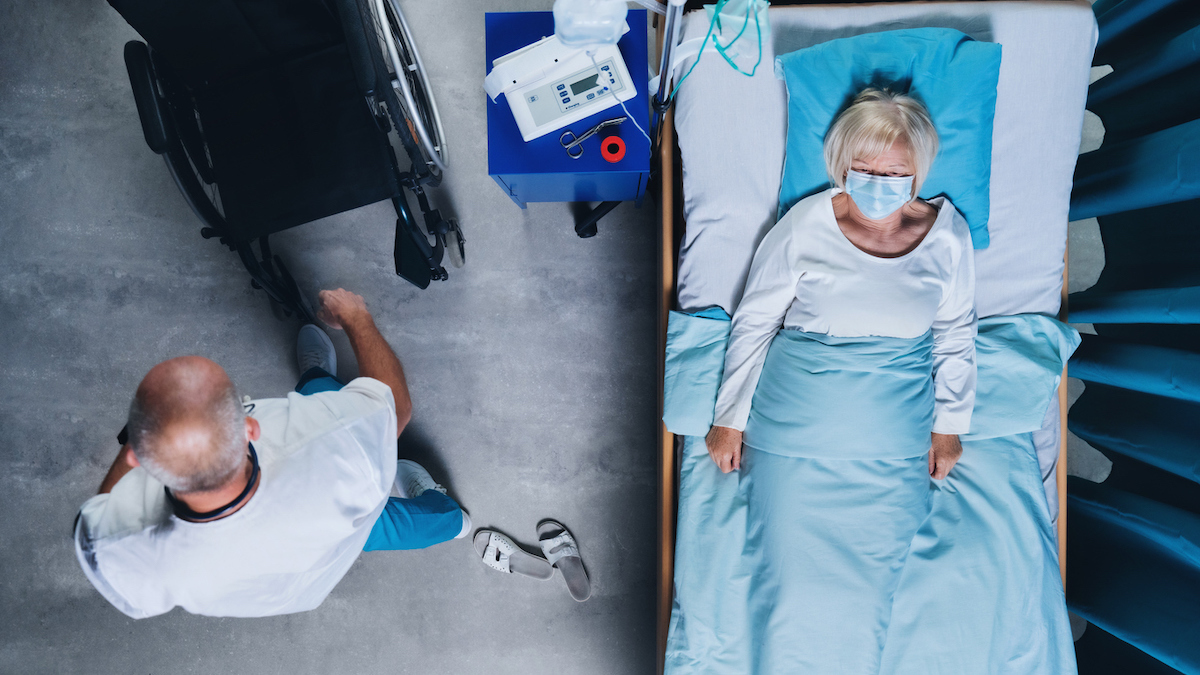
Während die Behandlung vorgeschlagen wird, um einen Patienten für einen Patienten zu verwenden, der in Richtung a fahren könntestarker Fall Von Covid und den Krankenhausaufenthalt stellt die FDA ausdrücklich fest, dass es nicht an Menschen verwendet wird, die bereits im Krankenhaus sind. "Bamlanivimab und Etevimab sind nicht für Patienten berechtigt, die aufgrund von COVID-19 ins Krankenhaus eingeliefert werden oder aufgrund von COVID Sauerstofftherapie erfordern", sagt die FDA.
Die Behandlung wurde nicht an den Krankenhauspatienten in Krankenhausträger untersucht. Pro FDA, "monoklonale Antikörper, wie Bamlanivimab und Etesevimab, können mit schlechteren klinischen Ergebnissen verbunden sein, wenn sie an einheimische Patienten mit COVID-19 verabreicht werden, die einen hohen Strömungssauerstoff oder eine mechanische Belüftung erfordern." Und um mehr Wege, um einen ernsthaften Fall von Coronavirus abzuheben,Dieses gemeinsame Medikament könnte Sie vor schweren Covid retten, sagt neue Studie.
Die Behandlung verringert das Risiko von COVID-Krankenhaus- und Todesrisiken um 70 Prozent.
Eli Lilly berichtete, dass im Januar eine Gerichtsverhandlung im Januar gezeigt hat, dass ihre Kombinationstherapiehalf, das Risiko zu reduzieren von Covid-staatlichen Krankenhausaufenthalten und Tod um 70 Prozent.
Die Behandlung wird sofort verfügbar sein. Laut Eli Lilly gibt es bereits 100.000 Dosen, die bereit sind, und weitere 150.000 Dosen im ersten Quartal zu erreichen. Das Unternehmen plant, bis Mitte des 2021 bis zu einer Million Dosen herzustellen. Und mehr über Ihr Coronavirus-Risiko,Wenn Sie dies getan haben, sind Sie doppelt so wahrscheinlich, dass sie schwere Covid entwickeln.
Und es ist nur ein Schuss.
Die Behandlung wird in einem einzigen Schuss verabreicht, der eine Kombination aus Bamlanivimab und Etevimab ist. Die FDA berichtet, dass er bei der Verwaltung von Covid-staatlichen Krankenhaus- und Todesfällen in den folgenden 29 Tagen im Vergleich zu einem Placebo erheblich reduziert.
Die Behandlung verwendet monoklonale Antikörper, die "laborgemachte Proteine sind, die die Fähigkeit des Immunsystems nachahmen, schädliche Erreger wie Viren zu bekämpfen." Bamlanivimab und Etesevimab werden speziell darauf ausgerichtet, gegen das Spike-Protein in Covid zu arbeiten, indem die Fähigkeit der Virus blockiert wird, an der Anhaftung und Einreise in menschliche Zellen einzugehen. Und für mehr Wege, um gesund zu bleiben,Diese 3 Vitamine könnten Sie vor schweren COVID sparen, Studienfunde.

Target fügt ab Sonntag neue Einschränkungen für den Selbstprüfungsuntersuchungen in 2.000 Geschäften hinzu

